Das Glow Stack Blend ist ein einzelnes lyophilisiertes Vial, das drei der meistuntersuchten Reparaturpeptide der modernen präklinischen Literatur in einer gemeinsamen Formulierung vereint: GHK-Cu (50 mg), TB-500 (10 mg) und BPC-157 (10 mg). Für Forschungsabläufe, in denen diese drei Substanzen bisher getrennt gehandhabt werden, reduziert das Blend drei Rekonstitutionsvorgänge auf einen und fixiert das Verhältnis der drei Peptide in einer definierten Stöchiometrie. Dieser Beitrag erläutert die biochemischen Rollen der drei Komponenten, die besonderen Anforderungen an die Rekonstitution eines kupferhaltigen Blends, die IE-Berechnung auf einer U100-Insulinspritze sowie die Frage, wann das Blend-Format einem Einzelvial-Ansatz tatsächlich überlegen ist. Alle nachfolgenden Angaben beziehen sich auf In-vitro- und Tiermodell-Forschung. Eine Anwendung am Menschen ist nicht vorgesehen und in Deutschland nicht zugelassen.
1. Was ist das Glow Stack Blend
Ein Peptid-Blend ist eine Kombination aus zwei oder mehr Peptiden, die gemeinsam in einem sterilen Vial gefriergetrocknet werden. Die forschende Person fügt einmalig bakteriostatisches Wasser zu, schwenkt das Gefäß behutsam und entnimmt im weiteren Verlauf alle Teilvolumina aus demselben Mehrdosenbehältnis. Das Glow Stack wird von Bergdorf Bioscience als HPLC-verifiziertes Forschungspeptid ausgeliefert und kombiniert die drei Wirkstoffe im Verhältnis 50 mg zu 10 mg zu 10 mg, was einem Gesamtgehalt von 70 mg aktivem Peptid pro Vial entspricht.
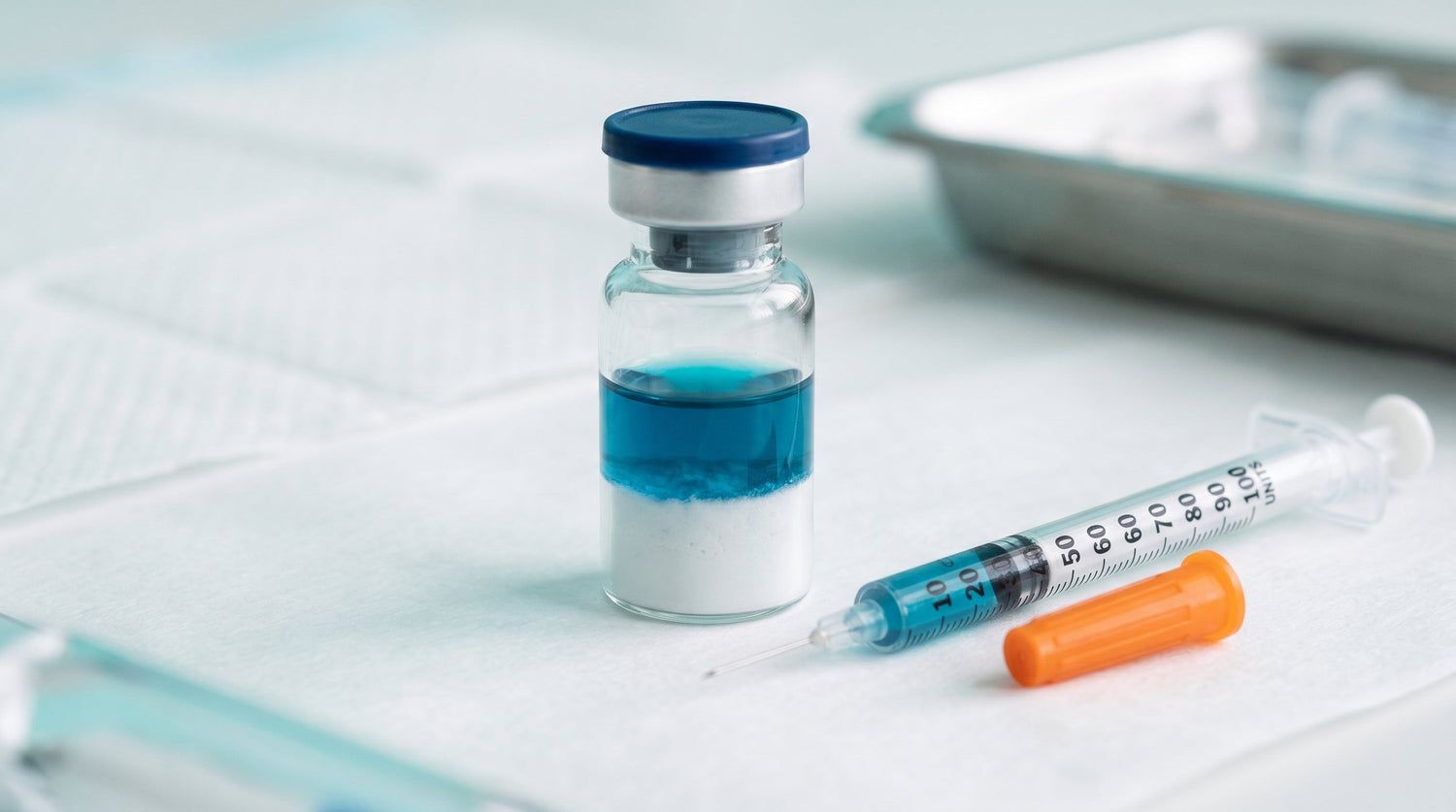
Die Namensgebung verweist auf die mechanistische Geschichte der Rezeptur, nicht auf kosmetische Werbeaussagen. GHK-Cu und TB-500 sind in der Literatur zur dermalen und bindegewebigen Reparatur breit dokumentiert, während BPC-157 vaskuläre und gastrointestinale Modelle in dieselbe Formulierung einbringt. Jede Komponente liegt als stabiler lyophilisierter Kuchen vor. Der charakteristische tiefblaue Farbton, der nach erfolgreicher Rekonstitution sichtbar wird, stammt vom GHK-Cu-Chelat und stellt das wichtigste visuelle Qualitätsmerkmal des gesamten Blends dar.
Zusammensetzung im Überblick
- GHK-Cu: 50 mg pro Vial. Tripeptid Glycyl-L-Histidyl-L-Lysin, komplexiert mit einem einzelnen Cu(II)-Ion. Theoretische Masse 340,79 Da.
- TB-500: 10 mg pro Vial. Synthetisches Fragment des Thymosin Beta-4, das die aktive Region LKKTETQ abdeckt. Vom Hersteller angegebene Halbwertszeit im Forschungsmodell ca. 7 Stunden.
- BPC-157: 10 mg pro Vial. Pentadekapeptid mit der Sequenz GEPPPGKPADDAGLV, abgeleitet aus einer vermuteten gastroprotektiven Sequenz. Angegebene Halbwertszeit ca. 4 Stunden.
- Gesamtpeptid: 70 mg.
- Darreichungsform: Weißes bis cremefarbenes lyophilisiertes Pulver unter inerter Gasatmosphäre.
- Angegebene Reinheit: HPLC-Reinheit von mindestens 99 Prozent pro Komponente, dokumentiert im chargenbezogenen Analysenzertifikat (CoA).
2. Wirkmechanismen der drei Peptide
Jede Komponente des Glow Stack besitzt eine eigene mechanistische Literaturbasis. Die drei Wirkpfade getrennt zu betrachten ist der einzige sachlich korrekte Weg, um einzuschätzen, was ein Blend in einem einzigen experimentellen Durchlauf liefern kann und was nicht.
GHK-Cu: Kupfertransport, ECM-Umbau und Redox-Modulation
GHK-Cu ist ein Koordinationskomplex aus dem Tripeptid Gly-His-Lys und einem Cu(II)-Ion. Loren Pickart isolierte das Molekül 1973 erstmals aus humanem Plasma. Der Komplex besitzt eine sehr hohe Affinität zu Kupfer (log K ca. 16,4) und gilt als physiologischer Kupfertransporter. In einem 2015 in BioMed Research International erschienenen Review fassten Pickart, Vasquez-Soltero und Margolina Connectivity-Map-Daten zusammen, nach denen GHK die Expression von rund 31 Prozent der profilierten humanen Gene in kultivierten Fibroblasten moduliert.
Die in der Literatur am konsistentesten beschriebenen nachgeschalteten Effekte umfassen die Induktion von Kollagen I und III, Elastin und Decorin (Maquart et al., FEBS Letters, 1988), eine Hochregulation der Transkripte von VEGF und bFGF, die Expressionserhöhung antioxidativer Enzyme wie SOD2 und diverser Metallothionein-Isoformen sowie eine Verschiebung des MMP-2- und TIMP-1/2-Gleichgewichts in Richtung eines nicht-fibrotischen Umbaus. Hostynek und Kollegen quantifizierten im Jahr 2010 die perkutane Absorption des intakten GHK-Cu-Komplexes durch humane Haut und stützten damit die Bioverfügbarkeit des Chelats als Einheit und nicht als isolierte Bestandteile.
TB-500: Aktin-Sequestrierung und Zellmigration
TB-500 ist die gebräuchliche Bezeichnung für ein synthetisches Fragment des Thymosin Beta-4 (Tb4), eines 43 Aminosäuren langen, aktinsequestrierenden Peptids, das in nahezu allen Säugerzellen vorkommt und das LKKTETQ-Motiv enthält. Das aktive Motiv bindet monomeres G-Aktin und moduliert die Aktin-Polymerisation am wandernden Zellpol. Bock-Marquette und Mitarbeiter berichteten 2004 in Nature, dass Tb4 das Überleben von Kardiomyozyten nach experimentellem Myokardinfarkt bei Mäusen über den PINCH/ILK/Akt-Signalweg fördert. Smart und Kollegen zeigten 2007, dass dasselbe Peptid adulte epikardiale Progenitorzellen mobilisiert.
In dermalen und kornealen Modellen beschleunigt Tb4 die Reepithelialisierung (Malinda et al., J Invest Dermatol, 1999; Sosne et al., Exp Eye Res, 2002), dämpft eine NF-kB-vermittelte Zytokinfreisetzung und reduziert die Myofibroblasten-Transdifferenzierung, was die Autoren als anti-narbigen Effekt interpretieren. Die langfristige onkologische Sicherheit ist eine offene Forschungsfrage, da dieselben migrations- und angiogenesefördernden Eigenschaften, die Wundverschlüsse unterstützen, in bestimmten murinen Melanommodellen mit einer erhöhten Metastasierungsrate korrelierten.
BPC-157: Stickstoffmonoxid, Angiogenese und Sehnenfibroblasten
BPC-157 (Body Protection Compound 157) ist ein Pentadekapeptid mit 15 Aminosäuren, das ab Beginn der 1990er Jahre von der Sikiric-Arbeitsgruppe an der Universität Zagreb beschrieben wurde. Der postulierte Mechanismus stellt die Modulation des Stickstoffmonoxid-Systems in den Mittelpunkt: BPC-157 wirkt einer L-NAME-induzierten eNOS-Blockade im Rattenmodell entgegen und fördert die Gefäßsprossung über eine VEGFR2-Internalisierung (Hsieh et al., J Mol Med, 2017). Chang und Kollegen zeigten 2011 im Journal of Applied Physiology, dass das Peptid die Expression des Wachstumshormonrezeptors auf Sehnenfibroblasten hochreguliert und deren Migration sowie Überleben in Kultur erhöht - ein Effekt, der in mehreren Modellen zur Achillessehnen- und Quadrizepssehnen-Durchtrennung bei Ratten reproduziert wurde. Sikiric und Mitarbeiter gaben 2010 in Current Pharmaceutical Design einen umfassenden Überblick über diese Datenlage.
BPC-157 zeichnet sich zusätzlich durch eine ungewöhnliche proteolytische Stabilität in Magensaft aus, was teilweise die Grundlage für orale Forschungsanwendungen bildet, auch wenn bisher keine humanen pharmakokinetischen Daten publiziert sind. Ein Großteil der Wirksamkeitsdaten stammt aus einer einzigen Forschungsgruppe, und unabhängige Replikationen der Studien mit größerer Effektstärke bleiben bisher begrenzt.
3. Synergiehypothese: ein Drei-Achsen-Modell
Keine peer-reviewte Studie hat bisher eine Paarkombination der drei Peptide GHK-Cu, TB-500 und BPC-157 in vitro oder in vivo getestet. Die Synergiebehauptung, die dem Glow Stack seine Legitimation verleiht, ist damit mechanistisch hergeleitet und nicht experimentell belegt. Die klarste Einordnung ist ein Drei-Achsen-Modell:
- Transkriptions-Achse (GHK-Cu): Hochregulation von VEGF, bFGF, Kollagen- und Elastintranskripten; Modulation des MMP/TIMP-Gleichgewichts via TGF-beta in Richtung eines nicht-fibrotischen ECM-Umbaus.
- Zytoskelett-Achse (TB-500): Sequestrierung von G-Aktin zur raschen Polymerisation am wandernden Zellpol; Unterstützung endothelialer Tubulogenese.
- Rezeptor- und NO-Achse (BPC-157): Förderung der VEGFR2-Internalisierung, Modulation der eNOS, Unterstützung des Turnovers fokaler Adhäsionen über FAK und Paxillin.
Da jedes der drei Peptide an einem anderen Knoten gemeinsam genutzter Signalwege angreift (VEGF-Achse, NF-kB-Suppression, ECM-Umbau), gilt die Kombination theoretisch als additiv und nicht redundant. Die sachliche Einschränkung lautet: "theoretisch additiv" ist nicht gleichbedeutend mit "experimentell additiv". Wer Synergie im eigenen Forschungsmodell belastbar darstellen möchte, muss die Kombination gegen die Einzelkomponenten testen. Das Blend senkt lediglich die Einstiegshürde für ein solches Experiment.
4. Rekonstitution eines kupferhaltigen Blends
Ein Blend mit GHK-Cu unterliegt nicht dem Standardprotokoll einer Peptidrekonstitution. Das Kupfer-Tripeptid-Chelat ist mechanisch und chemisch empfindlicher als TB-500 oder BPC-157 allein, weshalb das Protokoll an der empfindlichsten Komponente ausgerichtet werden muss.
Wahl des Lösungsmittels
Bakteriostatisches Wasser für Injektionszwecke (steriles Wasser mit 0,9 Prozent Benzylalkohol, BAC) ist das Standardlösungsmittel für ein Mehrdosen-Peptid-Blend. Reines steriles Wasser ist nur für Einzelentnahmen akzeptabel, da ihm das Konservierungsmittel für das mehrwöchige Entnahmefenster fehlt. Physiologische Kochsalzlösung (0,9 Prozent NaCl) ist zu vermeiden. Chloridionen konkurrieren um die Cu(II)-Koordination und beschleunigen die Transmetallierung des GHK-Cu-Chelats. Die Folge sind Trübungen, Farbverschiebungen oder sichtbare Ausfällungen innerhalb weniger Stunden. NaCl-Lösungen sind für zahlreiche Einzelpeptide unproblematisch, für jedes Vial mit einem Kupferpeptid jedoch das falsche Lösungsmittel.
Warum kein Vortex
Die wichtigste Handhabungsregel für das Glow Stack lautet: kein Vortexen, kein Schütteln, kein aggressives Pipettieren. Vortexen erzeugt eine Luft-Wasser-Grenzfläche und Scherkräfte, die Peptide über Schaumbildung und Kavitation denaturieren und teilweise das Cu(II) aus dem GHK-Chelat lösen. Das Zeichen eines geschädigten Blends ist eine Farbverschiebung vom charakteristischen tiefen Azurblau in Richtung Grün, Türkis oder Braun. Tritt diese ein, hat sich das Kupfer als Cu(OH)2 oder Hydrolyseprodukt aus dem Chelat gelöst, und die GHK-Cu-Komponente ist für Forschungszwecke nicht mehr verwendbar. Die beiden anderen Peptide können weiterhin intakt sein, das Blend als Ganzes hat jedoch die Komponente verloren, die ihm seinen Namen gab.
Die korrekte Methode ist die Schwenkmethode (Swirl-Methode). Der BAC-Wasserstrahl wird langsam entlang der inneren Glaswand des Vials eingeführt und nicht direkt auf den lyophilisierten Kuchen gerichtet. Das Vial wird anschließend für 30 bis 60 Sekunden zwischen den Handflächen geschwenkt oder gerollt, bis sich das Pulver vollständig auflöst. Bleibt ungelöstes Material zurück, wird das Vial für 10 bis 15 Minuten bei 2 bis 8 Grad Celsius gelagert und erneut geschwenkt. Die dafür aufgewendete Geduld schützt die teuerste Komponente im Vial.
pH-Kompatibilität
Das gemeinsame Stabilitätsfenster der drei Peptide liegt etwa zwischen pH 5,0 und 6,5. GHK-Cu ist im schwach sauren bis neutralen Bereich am stabilsten; oberhalb von etwa pH 7,4 beginnt das Cu(II)-Chelat, Kupfer freizusetzen, und die Lösung dunkelt sich. BPC-157 und TB-500 sind im gleichen Fenster gut löslich. BAC-Wasser hat von Natur aus einen pH-Wert um 5,5 und ist damit ohne zusätzliche Pufferung ein chemisch sinnvolles Lösungsmittel für das gesamte Blend.
5. IE- und Dosierungsberechnung für Forschende
U100-Insulinspritzen sind in internationalen Einheiten (IE) skaliert, wobei 100 IE einem Milliliter entsprechen, also 1 IE gleich 0,01 mL. Bei einem fixen Gesamtgehalt von 70 mg pro Vial hängt die Dosis pro IE ausschließlich vom gewählten Rekonstitutionsvolumen ab.
Konzentrationstabelle nach Rekonstitutionsvolumen
1 mL BAC-Wasser: GHK-Cu 50,0 mg/mL, TB-500 10,0 mg/mL, BPC-157 10,0 mg/mL.
2 mL BAC-Wasser: GHK-Cu 25,0 mg/mL, TB-500 5,0 mg/mL, BPC-157 5,0 mg/mL.
3 mL BAC-Wasser: GHK-Cu 16,67 mg/mL, TB-500 3,33 mg/mL, BPC-157 3,33 mg/mL.
Umrechnung pro IE auf einer U100-Spritze
Bei 2 mL Rekonstitution (typischer Forschungsstandard): 1 IE auf einer U100-Spritze entspricht 250 Mikrogramm GHK-Cu, 50 Mikrogramm TB-500 und 50 Mikrogramm BPC-157. Eine Entnahme von 20 IE liefert somit 5 mg GHK-Cu, 1 mg TB-500 und 1 mg BPC-157 in derselben Injektion von 0,20 mL.
Bei 1 mL Rekonstitution: Die Dosen pro IE verdoppeln sich. 1 IE entspricht 500 Mikrogramm GHK-Cu, 100 Mikrogramm TB-500 und 100 Mikrogramm BPC-157.
Bei 3 mL Rekonstitution: Die Dosen pro IE betragen etwa 167 Mikrogramm GHK-Cu, 33 Mikrogramm TB-500 und 33 Mikrogramm BPC-157. Der Nachteil liegt in der Genauigkeit: Je kleiner die Mikrogramm pro IE, desto verzeihender die Skalenschritte der Spritze, aber desto größer das Injektionsvolumen pro Forschungsereignis.
Halbwertszeit und Frequenzkonsequenzen
Die vom Hersteller angegebenen Halbwertszeiten im Forschungsmodell liegen bei ca. 12 Stunden für GHK-Cu, 7 Stunden für TB-500 und 4 Stunden für BPC-157. In einem koadministrierten Protokoll eliminieren die drei Komponenten aus einem einzigen Bolus mit unterschiedlichen Raten, was einen der legitimen Kritikpunkte an jedem Fix-Verhältnis-Blend darstellt: Die forschende Person kann die Applikationsfrequenz für die kurzlebigeren Komponenten nicht unabhängig titrieren, ohne zugleich die langlebigste mitzudosieren.
6. Lagerung und Stabilität
Lyophilisierte Vials werden kurz- bis mittelfristig lichtgeschützt bei 2 bis 8 Grad Celsius gelagert und für die Langzeitarchivierung über mehr als 30 Tage bei minus 20 Grad Celsius eingefroren. Der lyophilisierte Kuchen toleriert kurze Umgebungsversandfenster, da alle drei Peptide im Trockenzustand stabil sind. Das Vial sollte jedoch unmittelbar nach Eingang in eine Kühllagerung überführt werden.
Nach Rekonstitution in BAC-Wasser bleibt das Blend etwa vier Wochen bei 2 bis 8 Grad Celsius in stehendem Vial und unter Lichtschutz verwendbar. Die Stabilitätsobergrenze wird dabei von der GHK-Cu-Komponente vorgegeben. Die beiden anderen Peptide zersetzen sich langsam über Aspartat-Isomerisierung und Glutamin-Deamidierung; das Kupferchelat zerfällt schneller und vor allem sichtbarer. Das erste Zeichen einer Degradation ist eine Farbverschiebung von klarem hellblauem zu grün-braunem Ton, gefolgt von Trübung oder sichtbaren Partikeln. Diese Farbverschiebung ist ein Verwerfungssignal, selbst wenn der Kalender noch Restlaufzeit ausweist.
Drei Dinge sind bei einem rekonstituierten Blend grundsätzlich zu vermeiden: niemals wieder einfrieren, niemals in der Kühlschranktür lagern (dort treten bei jedem Öffnen Temperaturschwankungen auf) und niemals direktem Sonnenlicht aussetzen. Kupferpeptide sind in dem Maß lichtempfindlich, dass ein Braunglasvial oder eine Umhüllung mit Aluminiumfolie eine sinnvolle Vorsichtsmaßnahme für jedes Vial darstellt, aus dem über mehrere Wochen entnommen wird.
7. Glow Stack versus drei Einzelvials
Das Blend-Format ist nicht pauschal besser als drei einzelne Vials. Es stellt einen anderen Kompromiss dar. Die Stärken des Blends liegen in drei Bereichen: Es fasst einen Rekonstitutionsvorgang statt dreier zusammen, was die Wahrscheinlichkeit eines Aseptikfehlers an irgendeiner Stelle der Kette senkt. Es fixiert die drei Peptide in einem definierten Verhältnis, sodass eine einzige Entnahme von 0,20 mL eine feste Kombination liefert. Und es belegt einen Kühlschrankplatz statt dreier.
Drei Einzelvials gewinnen in puncto Flexibilität. Ein Studiendesign, das die GHK-Cu-Dosis unabhängig von TB-500 variieren muss, kann das aus dem Blend allein nicht leisten, ohne ein separates GHK-Cu-Vial hinzuzufügen. Ein Protokoll, das die Kombination gegen jedes Einzelpeptid vergleichen soll (der einzig ehrliche Weg, Synergie zu behaupten), benötigt die Einzelkomponenten ohnehin. Und die gemeinsame Vier-Wochen-Stabilitätsuhr nach Rekonstitution bedeutet: Endet das Experiment früher als geplant, altern die ungenutzten 60 Prozent des Blends gleichzeitig über alle drei Komponenten hinweg.
Die praktische Faustregel: Der Glow Stack ist das richtige Format, wenn das Verhältnis die experimentelle Konstante ist, und das falsche Format, wenn das Verhältnis selbst die zu untersuchende Variable darstellt. Wer ein lyophilisiertes 3-in-1 Peptid-Blend mit CoA als Ausgangspunkt prüfen möchte, kann dies tun, ohne sich die Option zu verschließen, später im Studienverlauf Einzelvials zu ergänzen.
8. Ausrüstung für subkutane Forschungsmodelle
Die Standardausrüstung für einen subkutanen Peptid-Forschungsworkflow ist kurz und in sich geschlossen. Das Blend ändert den Materialbedarf nicht; es reduziert nur die Zahl der Vials, die gleichzeitig in den Ablauf eingebracht werden.
- U100-Insulinspritzen, 0,5 mL Barrel, 30G oder 31G x 8 mm, idealerweise BD MICRO-FINE+ U100 0,5 ml Insulinspritzen für die kleinste Kanülengröße bei zuverlässiger IE-Kalibrierung.
- Bakteriostatisches Wasser für Injektionszwecke (Mehrdosen-Vial 30 mL, 0,9 Prozent Benzylalkohol).
- 70 Prozent Isopropanol-Alkoholtupfer, einen pro Septumeinstich und einen pro Injektionsstelle.
- Eine größere Rekonstitutionskanüle (21 bis 23G x 1 Zoll) und eine 3-mL-Spritze für den initialen BAC-Wasser-Transfer, die nicht für Dosierungen wiederverwendet werden darf.
- Einen zertifizierten Sharps-Behälter für die Einmalentsorgung von Kanülen.
- Puderfreie Nitrilhandschuhe und eine desinfizierte, ebene Arbeitsfläche.
- Ein Kühlschrank mit verifiziertem Temperaturbereich von 2 bis 8 Grad Celsius, idealerweise mit Thermometer oder Datenlogger für das Vier-Wochen-Entnahmefenster.
Einen abgestimmten Überblick über kompatibles Zubehör bietet die Injektions-Zubehör Sammlung, die Spritzen, Tupfer und Sharps-Behälter für Forschungsprotokolle bündelt.
9. Regulatorischer Rahmen in Deutschland und der EU
Keines der drei Peptide im Glow Stack ist in der Europäischen Union oder den Vereinigten Staaten als Arzneimittel für die humane therapeutische Anwendung zugelassen. In Deutschland regelt das Arzneimittelgesetz (AMG) den Verkehr mit Arzneimitteln; das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) ist die zuständige Bundesoberbehörde für die Zulassung und Überwachung von Arzneimitteln. Unzugelassene Peptide außerhalb legitimer Forschungskontexte können arzneimittelrechtliche Tatbestände nach dem AMG berühren. Zahlreiche Anbieter versenden ausschließlich unter der Auflage "nur für Forschungszwecke" und verlangen vom Empfänger eine Erklärung über die laborbezogene oder institutionelle Verwendung.
Andere europäische Behörden (ANSM in Frankreich, AEMPS in Spanien, AIFA in Italien, URPL in Polen) behandeln die unautorisierte humane Anwendung dieser Substanzen ebenfalls außerhalb des Zulassungsregimes. In den USA stuft die FDA die Verbindungen als Research Chemicals ein, solange sie explizit für Laborzwecke und nicht für den menschlichen Verzehr etikettiert sind.
TB-500 und BPC-157 werden zudem ausdrücklich unter WADA Code S0 (nicht zugelassene Substanzen) geführt, seit 2011 beziehungsweise 2019. Das bedeutet, dass ein Athlet in einem WADA-getesteten Wettkampf, der positiv auf eine der beiden Substanzen getestet wird, unabhängig von Intention oder Formulierung mit einer Sanktion rechnen muss. Praktisch bedeutet dies: Ein Glow-Stack-Vial in einem Forschungsumfeld ist ein In-vitro- und Tiermodell-Reagenz. Es ist in keinem der genannten Rechtsräume ein klinisches Produkt, und die begleitende Dokumentation sollte diese Tatsache abbilden.
10. Präklinische Evidenzbasis
Die peer-reviewte Literatur zu den drei Peptiden ist ungleich verteilt. GHK-Cu verfügt über die breiteste Basis mit mehreren Jahrzehnten an dermalen, trichologischen und kosmetischen Publikationen und einer soliden Grundlage in der Bindegewebsbiologie. TB-500, beziehungsweise das Mutterprotein Tb4, kann hochrangige Publikationen zu kardialen und kornealen Reparaturmodellen in Nature und JID vorweisen. Das synthetische LKKTETQ-Fragment selbst besitzt eine dünnere unabhängige Literaturdecke als das Volllänge-Protein. BPC-157 weist eine hohe Zahl an Publikationen in Sehnen-, Gastrointestinal- und Angiogenesemodellen auf, ist dabei jedoch stark auf eine einzelne Forschungsgruppe konzentriert; unabhängige Replikationen der großen Effektstärken stehen bisher nur begrenzt zur Verfügung.
Die sachliche Zusammenfassung: Die drei Peptide bewegen sich einzeln zwischen "interessante präklinische Substanz mit biologischer Plausibilität" und "frühphasige Forschungschemie mit unzureichender Humandatenlage". Das Blend ist eine Forschungsvereinfachung, kein evidenzbasiertes Upgrade. Wer die zugrundeliegenden Arbeiten selbst sichten möchte, findet über die PubMed-Suchen "GHK-Cu", "Thymosin beta 4 wound", "BPC-157 tendon" und "BPC-157 angiogenesis" die kanonischen Einstiegspunkte.
11. Qualitätsmerkmale bei der Bezugsquelle
Die Qualitätsbeurteilung eines Forschungspeptid-Vials lässt sich auf drei Dokumente und eine Beobachtung im Vial reduzieren:
- HPLC-Reinheitszertifikat: Umkehrphasen-HPLC-Chromatogramm mit einem dominanten Peak pro Komponente, integrierte Fläche angegeben, Zielwert mindestens 99 Prozent.
- Massenspektrometrische Identität: ESI-MS oder MALDI-TOF bestätigt die theoretische monoisotope Masse jedes Peptids. GHK-Cu ca. 340,79 Da, BPC-157 ca. 1419,55 Da, das TB-500-Fragment je nach verwendeter Sequenz im Bereich 2,5 bis 3,0 kDa.
- Chargenbezogenes CoA: pro Charge HPLC-Reinheit, MS-Ergebnis, Peptidgehalt (typischerweise 70 bis 90 Prozent über Aminosäureanalyse), Wassergehalt (Karl-Fischer, unter 8 Prozent) und Acetat-Gegenionengehalt.
- Der Blautest: Nach Rekonstitution sollte die GHK-Cu-Komponente dem Vial einen klaren, tiefen azurblauen Farbton verleihen. Eine blasse, grünliche, braune oder trübe Lösung ist ein Vorwarnsignal, auch wenn die Dokumentation einwandfrei erscheint.
Anbieter, die chargengenaue CoAs veröffentlichen und Drittanalysen durch unabhängige Peptidlabore (Janoshik Analytical, Anabolic Lab und vergleichbare) akzeptieren, gelten praktisch als Goldstandard im Forschungspeptid-Segment. Wer Bezugsquellen vergleicht, sollte die auf dem Vial-Etikett gedruckte CoA-Chargennummer gegen das zugehörige Dokument abgleichen; Abweichungen sind ein eindeutiges Verwerfungssignal. Bergdorf Bioscience Forschungspeptide werden mit chargengebundener HPLC- und MS-Dokumentation gemäß der veröffentlichten Produktspezifikation vertrieben.
12. Häufig gestellte Fragen
Kann das Glow Stack mit physiologischer Kochsalzlösung rekonstituiert werden?
Nein. Kochsalzlösung (0,9 Prozent NaCl) sollte vermieden werden, da Chloridionen um die Cu(II)-Koordination konkurrieren und das GHK-Cu-Chelat destabilisieren. Bakteriostatisches Wasser für Injektionszwecke ist das Standardlösungsmittel für jedes Blend mit einem Kupferpeptid.
Warum erscheint das rekonstituierte Blend blau?
Die blaue Farbe stammt vom GHK-Cu(II)-Chelat. Eine klare, tiefe azurblaue Lösung ist das erwartete Erscheinungsbild nach korrekter Rekonstitution. Eine grünliche, türkise oder bräunliche Verfärbung deutet darauf hin, dass sich Kupfer aus dem Chelat gelöst hat, und ist ein Verwerfungssignal.
Kann das Vial per Vortex schneller gelöst werden?
Nein. Vortexen erzeugt Scherkräfte und Schaum, die Peptide denaturieren und das GHK-Cu-Chelat dissoziieren lassen. Korrekt ist die Schwenkmethode: BAC-Wasser an der Vialwand herablaufen lassen und das Vial für 30 bis 60 Sekunden zwischen den Handflächen schwenken oder rollen.
Wie lange hält das rekonstituierte Glow Stack im Kühlschrank?
Etwa vier Wochen bei 2 bis 8 Grad Celsius, stehend und lichtgeschützt. Die Stabilitätsobergrenze ergibt sich aus der GHK-Cu-Komponente; verlässt die Farbe das Azurblau bereits vor Ablauf der vier Wochen, ist früher zu verwerfen.
Kann das rekonstituierte Blend eingefroren werden, um die Haltbarkeit zu verlängern?
Nein. Frier-Tau-Zyklen stören das Kupferchelat und schneiden Peptidbindungen. Wenn eine längere Lagerung erforderlich ist, sollte das lyophilisierte Pulver vor der Rekonstitution in kleine Portionen aliquotiert und dann bedarfsgerecht einzeln gelöst werden.
In welcher Konzentration sollte rekonstituiert werden?
2 mL BAC-Wasser gelten als typischer Forschungsstandard und ergeben 25 mg/mL GHK-Cu sowie jeweils 5 mg/mL TB-500 und BPC-157. Kleinere Volumina erhöhen die Dosis pro IE und erlauben kleinere Entnahmen; größere Volumina verbessern die Dosiergranularität auf Kosten eines größeren Injektionsvolumens.
Warum ein Blend statt drei Einzelvials?
Ein Rekonstitutionsvorgang statt dreier reduziert das Aseptikrisiko, ein Kühlplatz statt dreier, und ein fixiertes Verhältnis für Protokolle, in denen das Verhältnis konstant gehalten wird. Drei Einzelvials bleiben vorteilhaft, wenn das Design eine unabhängige Variation der Komponenten erfordert.
Gibt es eine publizierte Studie zu GHK-Cu, TB-500 und BPC-157 in Kombination?
Nein. Keine peer-reviewte Arbeit hat eine Paarkombination der drei Peptide getestet. Die Synergiebehauptung ist mechanistisch hergeleitet und stützt sich darauf, dass die drei Peptide an unterschiedlichen Knoten überlappender Signalwege (VEGF, NF-kB, ECM-Umbau) angreifen. Wer experimentelle Synergie belegen möchte, muss die Kombination im eigenen Modell gegen die Einzelkomponenten testen.
Welche Kanülengröße ist geeignet?
Für subkutane Forschungsmodelle ist eine U100-Insulinspritze 30G oder 31G x 8 mm Standard. Die BD MICRO-FINE+ 0,5 mL ist weit verbreitet und bietet eine zuverlässige IE-Kalibrierung; kleinere Barrels (0,3 mL) tauschen Gesamtvolumen gegen feinere Skalenstriche.
Sind TB-500 und BPC-157 im WADA-getesteten Sport verboten?
Ja. Beide Substanzen fallen unter WADA Code S0, die Kategorie der nicht zugelassenen Substanzen. Jeder Athlet in einem WADA-getesteten Wettkampf, der auf eines der beiden Peptide positiv getestet wird, muss unabhängig von Formulierung oder Absicht mit einer Sanktion rechnen. Das Glow Stack wird ausschließlich für In-vitro- und Tiermodell-Forschung angeboten.
Was geschieht bei einer Überdosierung in einem Forschungsmodell?
Die akute Toxizität der drei Peptide wird in Tierstudien einzeln als niedrig beschrieben, zur Koadministration liegen jedoch nur wenige Daten vor. Jedes Tierversuchsprotokoll sollte definierte humane Endpunkte, tierärztliche Aufsicht und eine Genehmigung der zuständigen Tierschutzbehörde vor Beginn beinhalten.
Wo kann das Blend mit dokumentiertem Analysenzertifikat bezogen werden?
Bergdorf Bioscience liefert das Glow Stack Blend mit einem chargengebundenen HPLC- und MS-Zertifikat. Die CoA-Chargennummer sollte bei Eingang gegen das Vial-Etikett abgeglichen werden; bei abweichenden Chargennummern ist die Annahme zu verweigern.
13. Medizinischer Haftungsausschluss
Dieser Blogbeitrag dient ausschließlich Informationszwecken und ersetzt keine professionelle medizinische Beratung. GHK-Cu, TB-500 und BPC-157 sind experimentelle Peptide und in der Europäischen Union, den Vereinigten Staaten sowie den meisten weiteren Rechtsräumen nicht für die humane Anwendung zugelassen. Gemäß dem deutschen Arzneimittelgesetz (AMG) handelt es sich um experimentelle Präparate, die nicht für die humane Nutzung zugelassen sind. Die Verwendung außerhalb klinischer Studien oder zugelassener Indikationen ist in vielen Jurisdiktionen illegal. TB-500 und BPC-157 sind zudem ausdrücklich unter WADA Code S0 als nicht zugelassene Substanzen gelistet.
Alle Angaben zu Wirkmechanismen, Rekonstitution, Dosierungsberechnungen und Lagerung stützen sich auf verfügbare präklinische Forschung und Herstellerdokumentation und können unvollständig oder ungenau sein. Individuelle Reaktionen, Sicherheitsprofile und pharmakokinetische Parameter können zwischen Spezies sowie zwischen In-vitro- und In-vivo-Modellen erheblich variieren. Die in diesem Artikel beschriebenen Rekonstitutionsberechnungen und IE-Äquivalente beziehen sich auf physische Konzentrationen im Vial und nicht auf humane therapeutische Dosen.
Bevor ein Peptid in einem Forschungsmodell eingesetzt wird, sind die zuständige Ethikkommission, die Tierschutzkommission und die Biosicherheitsstelle zu konsultieren. Dieser Artikel befürwortet weder die Off-Label-Anwendung noch die illegale Nutzung der diskutierten Substanzen. Der Autor und parahealth übernehmen keine Haftung für Nebenwirkungen, Verletzungen, regulatorische Konsequenzen oder nachteilige Ereignisse, die sich aus der Nutzung der in diesem Beitrag enthaltenen Informationen ergeben.
Nur für Forschungszwecke. Nicht für den menschlichen Verzehr bestimmt. Es gilt das jeweilige nationale Recht.

Kommentar hinterlassen
Alle Kommentare werden vor der Veröffentlichung moderiert.
Diese Website ist durch hCaptcha geschützt und es gelten die allgemeinen Geschäftsbedingungen und Datenschutzbestimmungen von hCaptcha.